UDI Management in meddevo
Basic UDI-DI - Allgemeine Informationen
Die Basis-UDI-DI ist ein eindeutiger Code, der ein Produktmodell oder eine Produktfamilie identifiziert und als Hauptschlüssel für Datensätze in der europäischen Datenbank EUDAMED dient. Sie wird nicht direkt auf dem Produkt oder seiner Verpackung angebracht, sondern ist eine reine Verwaltungs- und Datenbankkennung, die für administrative und regulatorische Zwecke benötigt wird. Die Basis-UDI-DI ist unabhängig von einzelnen Verpackungseinheiten und wird benötigt, um mehrere UDI-DIs (Geräteidentifikationen) zu einer Gruppe zusammenzufassen.
Wofür die Basis-UDI-DI zuständig ist:
Gruppierung von Produkten:
Sie verbindet Medizinprodukte mit demselben Verwendungszweck, derselben Risikoklasse sowie ähnlichen Design- und Herstellungsmerkmalen.
Hauptschlüssel in EUDAMED:
Sie ist der primäre Schlüssel zur Identifizierung von Produktgruppen in der EUDAMED-Datenbank.
Verknüpfung von Dokumenten:
Sie ist in relevanten Dokumenten wie Konformitätserklärungen und technischen Unterlagen zu finden.
Was die Basis-UDI-DI nicht ist:
- Nicht auf Produkten: Sie wird nicht auf dem Produkt selbst oder dessen Verpackung angebracht.
- Keine Produkt- oder Verpackungsidentifikation: Sie ist keine Kennung für eine spezifische Einheit, sondern für eine Gruppe von Geräten.
Unterschied zur UDI-DI:
- Die Basis-UDI-DI identifiziert eine ganze Produktfamilie oder einen Produktmodell.
- Die UDI-DI identifiziert jedes einzelne Produkt innerhalb dieser Familie und wird auf das Produkt oder die Verpackung aufgebracht.
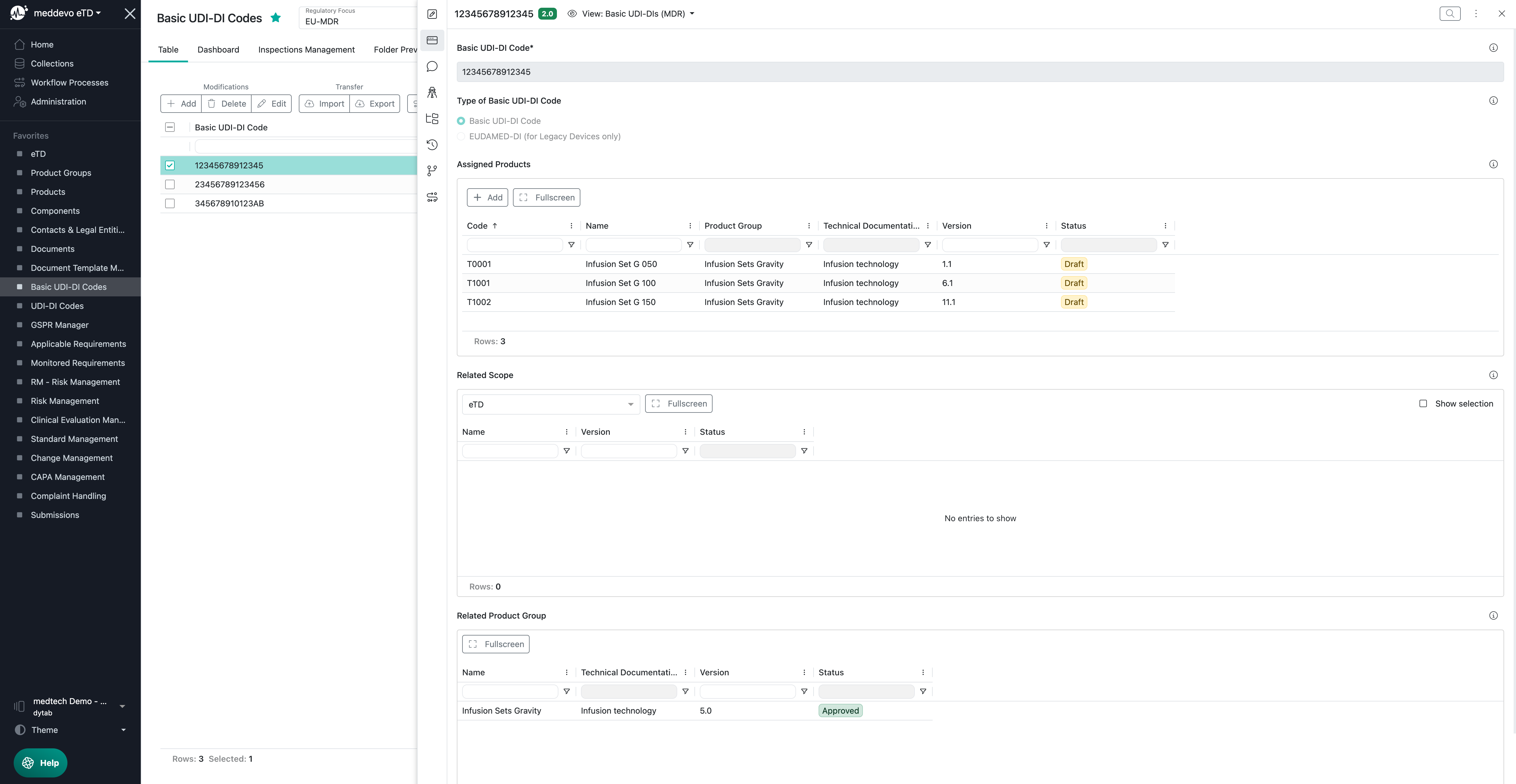
Basis UDI-DI-Codes und relevante Informationen in meddevo
Die Sammlung der Basis UDI-DI-Codes ist der Ort, an dem Sie Ihre Codes verwalten können:
Natürlich können Sie alle Ihre Basis UDI-DI Codes über einen Excel-Import importieren.
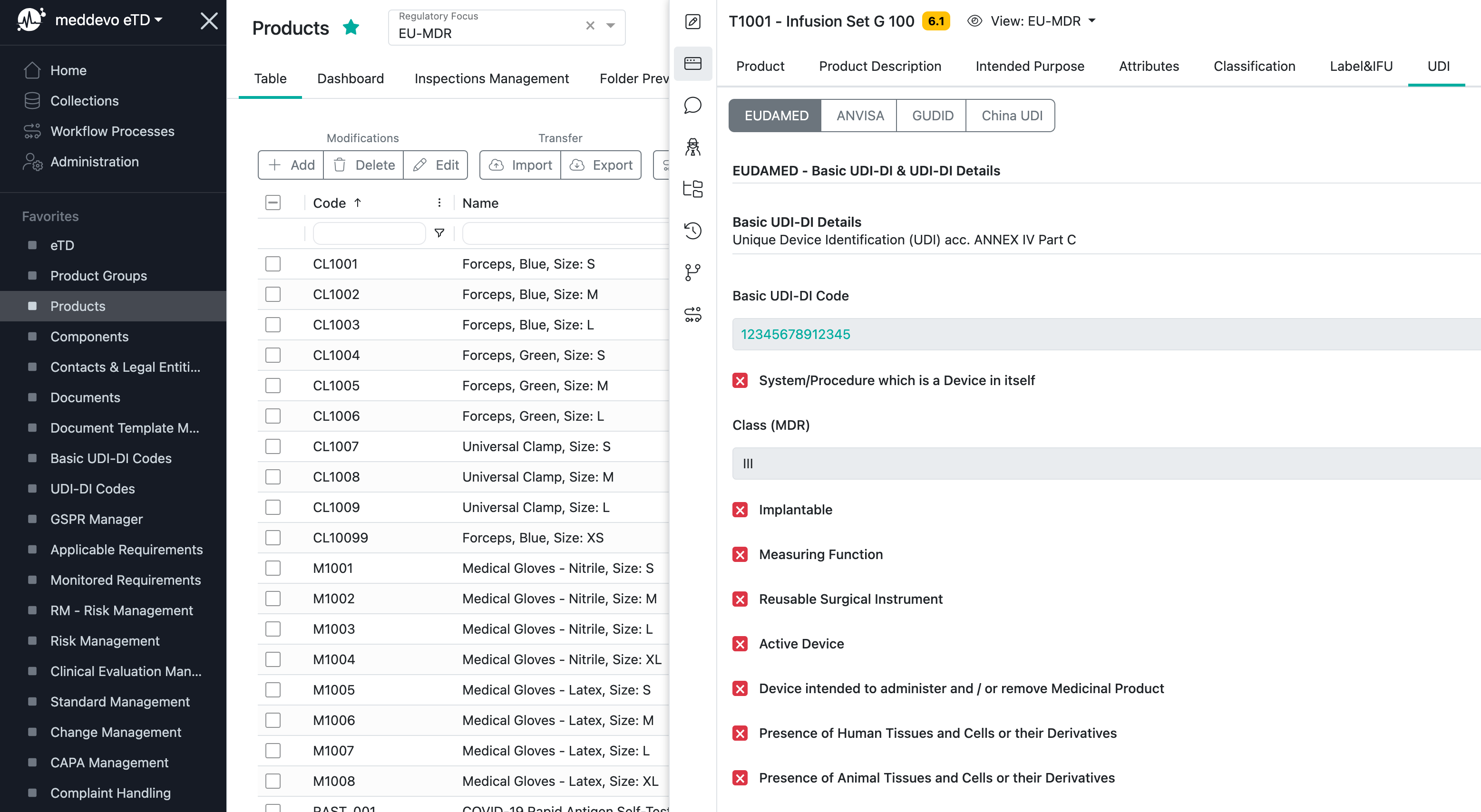
Alle grundlegenden regulatorischen Informationen zum Basis UDI-DI-Code werden in Ihrer Produktsammlung verwaltet:
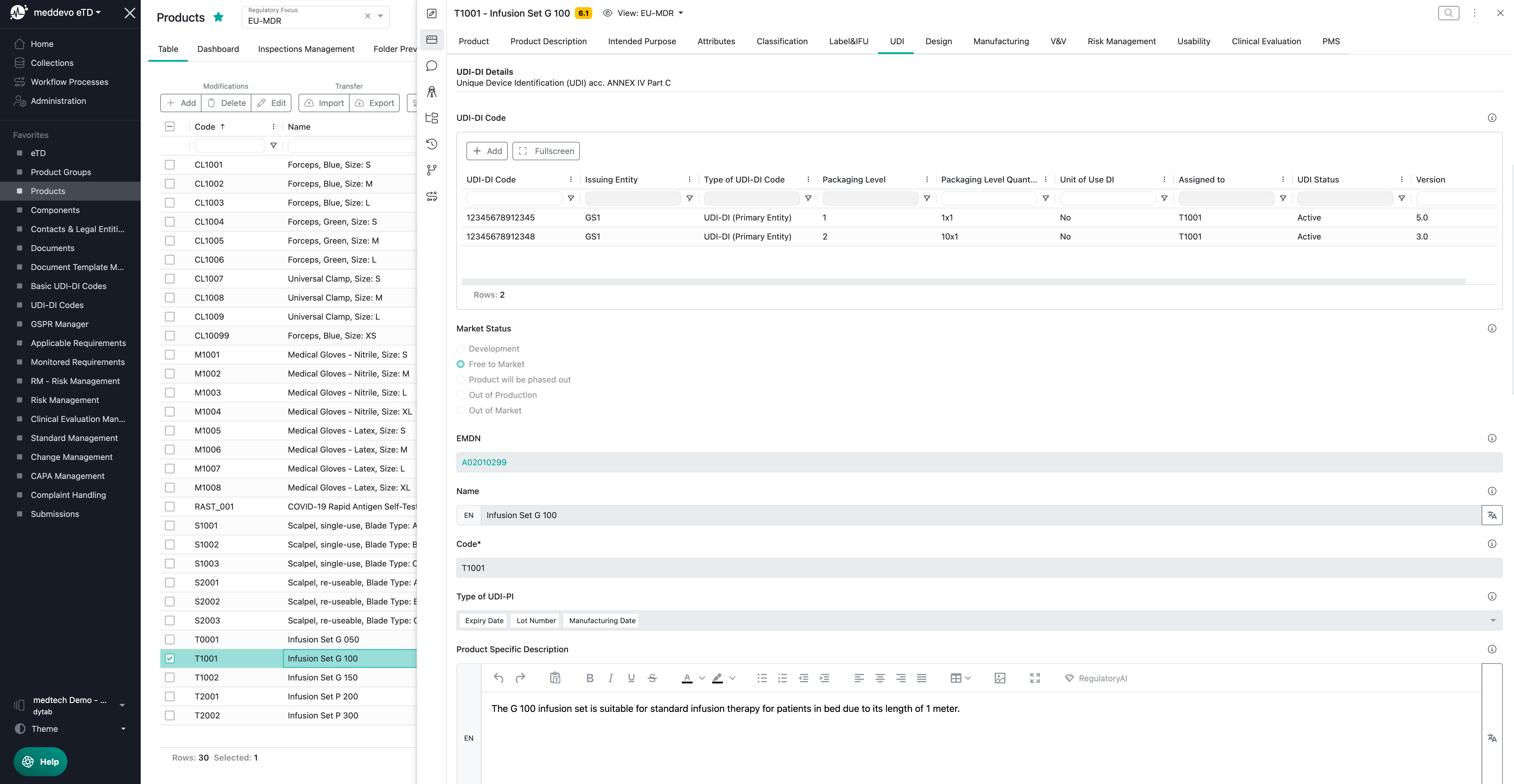
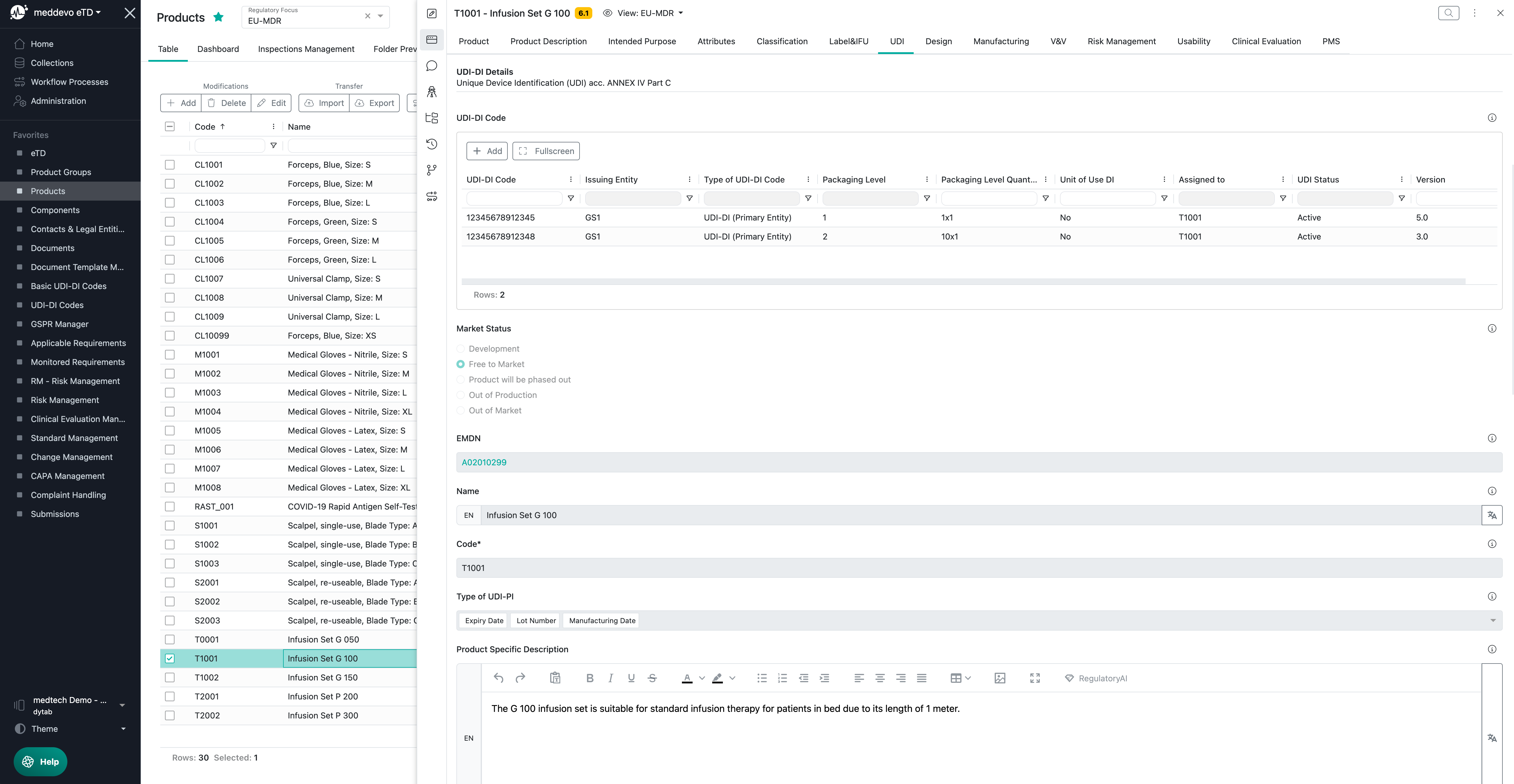
UDI-DI-Codes und relevante Informationen in meddevo
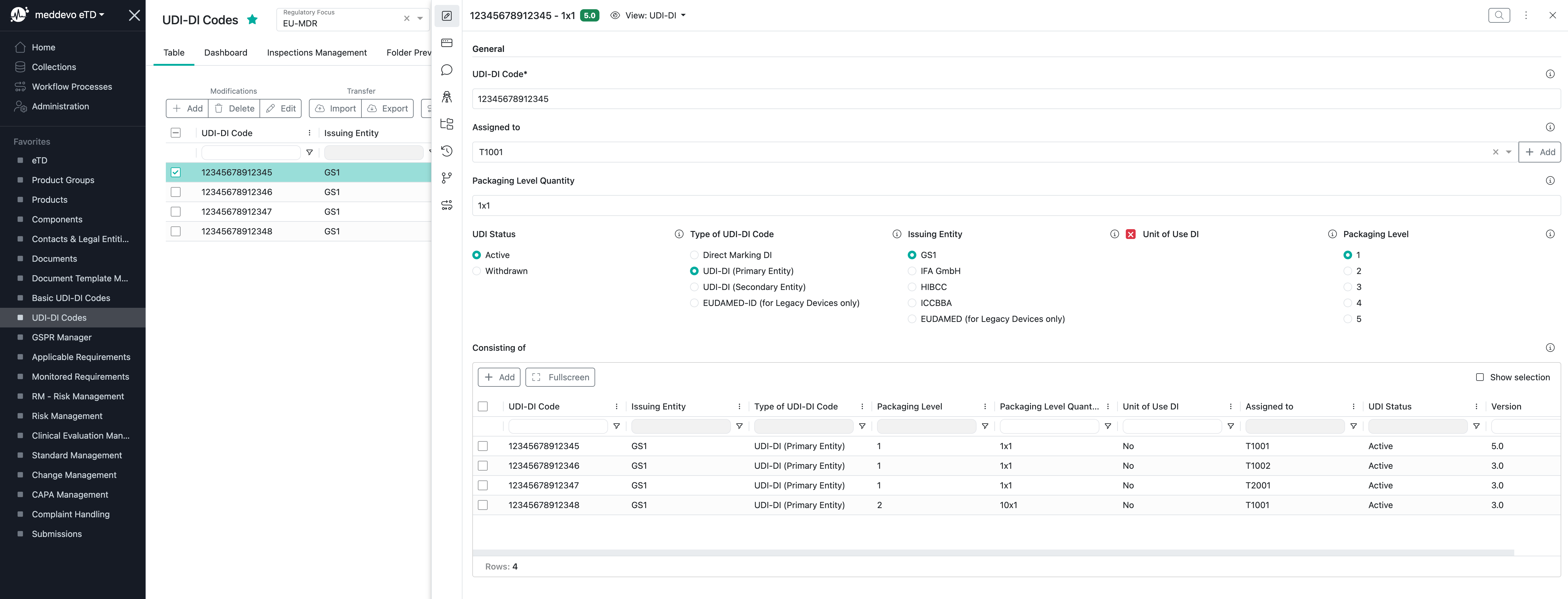
Die UDI-DI-Codes-Sammlung ist der Ort, an dem Sie Ihre Codes und EUDAMED relevante Attribute verwalten können:
Natürlich können Sie alle Ihre UDI-DI Codes über einen Excel-Import importieren.
Beschreibung und Erläuterung der UDI-DI-relevanten Felder:
- „UDI-DI-Code“ – hier können Sie Ihren UDI-DI-Code eingeben.
- „Zugewiesen zu“ – hier können Sie das mit dem UDI-DI-Code verknüpfte Produkt zuweisen.
- „Verpackungsmenge“ – hier können Sie die Menge Ihrer Verkaufseinheit festlegen, z. B. 1x1, 10x1, 30x5 usw.
- „UDI-Status“ – hier können Sie festlegen, ob der UDI-DI-Code zurückgezogen wurde oder noch aktiv ist.
- „Art des UDI-DI-Codes“ – hier können Sie zwischen folgenden Optionen unterscheiden:
- Direkte Kennzeichnung DI – wenn Sie ein wiederverwendbares Produkt haben, das eine direkte Kennzeichnung erfordert
- UDI-DI (primäre Stelle) – wenn Sie Ihre Standard-UDI-DI-Codes verwenden, die von Ihrer ersten ausstellenden Stelle angeboten werden
- UDI-DI (sekundäre Stelle) – wenn Sie zwei ausstellende Stellen parallel haben
- EUDAMED-ID (nur für Altgeräte) – wenn Sie Ihre Altgeräte registrieren müssen
- „Ausstellende Stelle“ – hier können Sie eine der fünf offiziellen UDI-ausstellenden Stellen auswählen.
- „Verwendungseinheit DI“ – dies ist nur erforderlich, wenn Ihre kleinste Verkaufseinheit mehr als ein Produkt enthält. In diesem Fall müssen Sie eine Verwendungseinheit DI definieren, die physisch nicht auf Ihrem Produkt verfügbar ist. Dies ist nur für EUDAMED und Kundenreklamationen erforderlich.
- „Verpackungslevel“ – hier definieren Sie die verschiedenen Verpackungsstufen Ihrer offiziellen Verkaufseinheiten. Versandkartons und -container werden nicht berücksichtigt.
- Zum Beispiel:
- Primärverpackung (Level 1) mit dem Inhalt 1x1 (definiert unter Verpackungsmenge)
- Sekundärverpackung (Level 2) mit dem Inhalt 5x1
- Tertiärverpackung (Level 3) mit dem Inhalt 30x5.
- Paletten bzw. aller logistischen Verpackungsebenen sind nicht relevant.
- Zum Beispiel:
- „Bestehend aus“ – wenn Sie eine UDI-DI für eine höhere Verpackungsebene definieren, können Sie hier die entsprechenden UDI-DI-Codes der unteren Ebenen desselben Produkts auswählen.
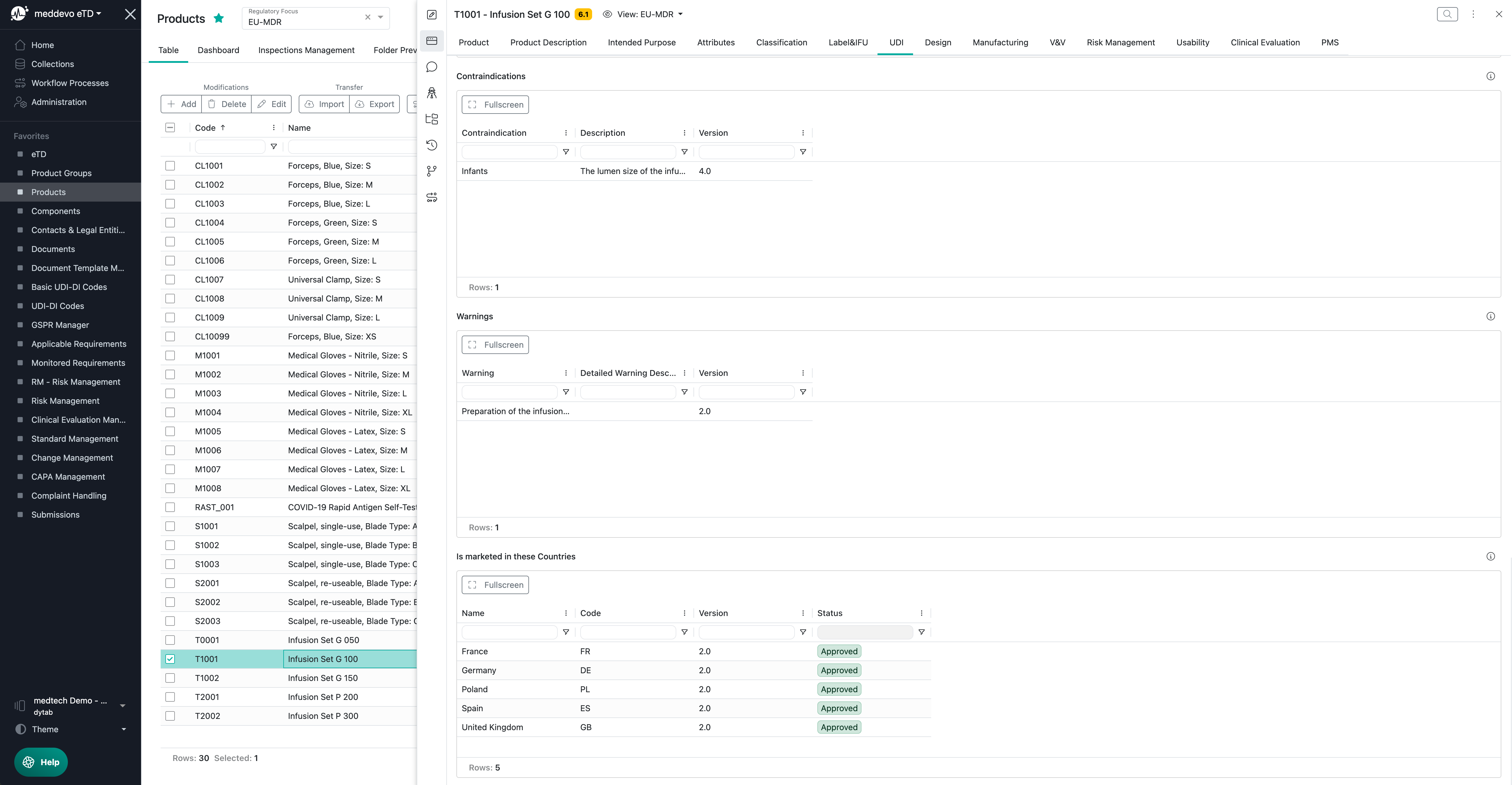
Alle für den UDI-DI-Code relevanten regulatorischen Informationen, die für die EUDAMED Registrierung benötigt werden, werden in der Sammlung "Produkte" verwaltet und in dem Bereich "UDI" zusammengefasst: